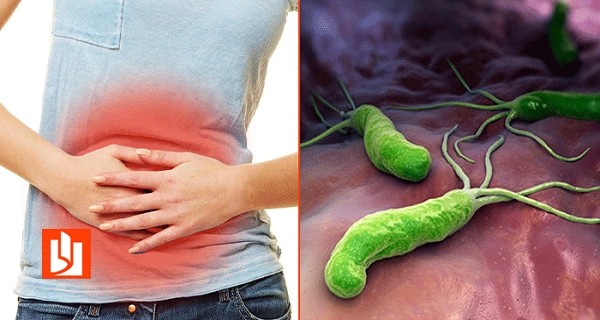
Незабаром весняний період змусить нас приділити більше уваги когорті пацієнтів із патологією шлунково-кишкового тракту, пов’язаною із інфекцією H. pylori (хелікобактер пілорі).
Найчастіше, це пацієнти із загостренням хронічного гастриту (ХГ) та виразкової хворобою (ВХ) шлунку та дванадцятипалої кишки, типовий варіант перебігу яких передбачає сезонність загострень: весна та осінь. Серед інших критеріїв «типового» перебігу чільне місце займає інфікування H. pylori, який є причиною даних захворювань і без знищення його в організмі не можливо досягти клінічної ремісії H. pylori-асоційованих захворювань і попередити їх рецидив.
Інфікуватись H. pylori можливо при вживанні їжі у закладах громадського харчування, поїздах за умов недотримання санітарно-гігієнічних вимог обробки столових приборів (забруднені H. pylori від попереднього відвідувача), у побуті (сімейний тип інфікування, у разі, якщо член родини інфікований і користується спільним посудом, при поцілунках тощо), під час ендоскопії (за відсутності належної дезінфекції ендоскопів – експозиції у спеціальному дезрозчині упродовж 15 годин) тощо. H. pylori є в зубному нальоті, слині, у шлунковому, кишковому вмісті та випорожненнях. Тому дану інфекцію можна віднести також і до хвороб «немитих рук».
У жовтні 2016 року в журналі «Gut» були опубліковані нові рекомендації Маастрихтського консенсусу (V) (Management of Helicobacter pylori infection – the Maastricht V / Florence Consensus Report). Метою останніх дискусій експертів була вироблення найбільш обгрунтованої і сучасної (state-of-the-art) настанови з діагностики, лікування та профілактики хелікобактерної інфекції.
Сьогодні відомо, що H. pylori, колонізуючи шлунок, викликає гастрит у всіх людей. Залежно від факторів вірулентності, сприйнятливості макроорганізму і способу життя ця інфекція може мати різні наслідки – від безсимптомного перебігу (80% випадків) до розвитку злоякісних новоутворень.
Helicobacter pylori – мікроаерофільна, Грам-негативна бактерія, S-подібної форми. Н. pylori виявляють у 100% хворих на виразкову хворобу ДПК, і близько 90% хворих на виразкову хворобу шлунка. H. pylori викликає хронічний активний гастрит у всіх інфікованих пацієнтів. Надалі він потенційно може призвести до виразкової хвороби, атрофічного гастриту, раку шлунка і MALT-лімфоми. Успішна ерадикація (повне знищення) H. pylori попереджує прогресування та рецидивування захворювань.
Кіотський глобальний консенсус із хелікобактерного гастриту визначає H. pylori-гастрит як самостійне інфекційне захворювання. У Маастрихті V також зазначається, що H. pylori-гастрит є інфекційним захворюванням незалежно від наявності симптомів та ускладнень, і лікарі зобов’язані встановити цей діагноз не залежно від того турбують дану особу будь-які симптоми чи ні.
Н.pylori-асоційований гастрит – органічне захворювання на відміну від функціональної диспепсії, яка є функціональним захворюванням. У Маастрихтському консенсусі V вказано, що діагноз істинної функціональної диспепсії повинен встановлюватися лише за відсутності H. рylori або після його успішної ерадикації.
Н.pylori-асоційований гастрит може викликати симптоми диспепсії (порушення травлення) у частини пацієнтів. Ерадикація H. pylori здатна зменшити прояви диспепсії. Алгоритм діагностики H. pylori-асоційованої диспепсії є доволі простим. У разі наявності диспепсії та виявлення H. pylori призначається лікування – ерадикаційна терапія. За умови стійкого полегшення (після 6-12 міс) діагностується H. pylori-асоційована диспепсія. Якщо симптоми рецидивують або не змінюються, у пацієнта наявна функціональна диспепсія. При недослідженій диспепсії може застосовуватися стратегія test-and-treat («діагностуй і лікуй»).
Найважливішим завданням ерадикації H. pylori є запобігання раку шлунка.
Вважається, що 90% випадків розвитку раку шлунка пов’язані з хелікобактерної інфекцією. Щорічно у світі діагностується майже 1 млн випадків цього захворювання. Підвищений ризик раку шлунку мають пацієнти з фенотипом Са шлунку — наявність гастриту тіла шлунку, атрофії і кишкової метаплазії, гіпохлоргідрії, хелікобактерної інфекції у минулому або наразі. Успішна ерадикація H. pylori здатна зменшити ризик розвитку раку шлунка, що доведено у великих міжнародних дослідженнях.
Пацієнти з такими захворюваннями повинні виявлятися і лікуватися. Пацієнти з атрофією і кишковою метаплазією повинні підлягати ендоскопічному (гастродуоденогастрофіброскопія) і морфологічному дослідженням. Ерадикація H. pylori здатна зменшити прояви атрофії слизової оболонки, зворотній розвиток кишкової метаплазії після ерадикації не досягається. Однак вона не прогресує.
Вживання хворими на ревматологічну, неврологічну патологію ліків з групи нестероїднах протизапальних засобів (НПЗП) із протизапальною, знеболювальною, антитромбоцитарною метою, у т.ч. ацетилсаліцилової кислоти (аспірину), інших антиагрегантів, у яких в організмі є H. рylori – це незалежні фактори ризику розвитку пептичної виразки та її ускладнень. Доведений феномен взаємообтяження H. pylori у НПЗП-користувачів із потенціюванням звиразкування слизової оболонки ШКТ та зростання ризику кровотеч.
Консенсус рекомендує тестувати на H. рylori пацієнтів, які приймають НПЗП і аспірин, з наявністю в анамнезі пептичної виразки, а також рекомендує призначення антисекреторних препаратів для захисту слизової оболонки, а при виявленні бактерії – антихелікобактерну терапію.
Доведений взаємозвязок H. рylori із
- залізодефіцитною анемією,
- ідіопатичною тромбоцитопенічною пурпурою
- В12-дефіцитною анемією
- MALT-лімфомою, аденокарциномою шлунку
У яких випадках необхідно проводити діагностику та ерадикацію Н.р.?
- Бажання пацієнта
- Пептичні виразки шлунка та ДПК
- MALT-лімфома
- Неатрофічний гастрит, атрофічний гастрит
- Стан після резекції шлунка з приводу карциноми
- Перший ступінь родинності з хворим на рак шлунка,
- Недосліджена функціональна диспепсія
- Терапія НПЗП, глюкокортикоїдними гормонами, антиагрегантами, антикоагулянтами
- Тривала терапія гастроезофагеальної рефлюксної хвороби (ГЕРХ) із застосуванням інгібіторів протонної помпи
- Ішемічна хвороба серця
- Імунна тромбоцитопенічна пурпура
- Залізодефіцітна анемія, що немає пояснення
Методи діагностики Helicobacter pylori
1. Біохімічні методи:
швидкий уреазний тест,
уреазний дихальний тест з 13С-сечовиною,
амонійний дихальний тест.
2. Морфологічні методи:
2.1. гістологічний метод
2.2. цитологічний метод
3. Імунологічні методи:
3.1. виявлення антигену H.pylori у калі .
3.2. виявлення антитіл до H.pylori у крові .
4. Мікробіологічний метод (чутливість до антибіотиків)
5. Молекулярно-генетичні методи:
ПЛР при дослідженні біоптатів слизової оболонки шлунка.
При проведенні ендоскопії при діагностиці виразкової хвороби, гастриту, функціональної диспепсії, ГЕРХ необхідне тестування на H.pylori. Методом вибору є швидкий уреазний тест (90% чутливість, 95–100% специфічність).
Маастрихтський консенсус V рекомендує не використовувати швидкі серологічні тести для визначення ефективності лікування – виявляють не лише реальну, але і колишню (вилікувану) інфекцію.
Для оцінки ефективності ерадикаційної терапії рекомендовані 13С-уреазний дихальний тест або визначення антигену H. pylori в калі через 4–8 тижнів після закінчення терапії.
Згідно з рекомендаціями міжнародного консенсусу Маастрихт V (2016) та Кіотського консенсусу (2015), використовуються трьох- або чотирьохкомпонентні варіанти ерадикаційної терапії H. pylori. Важливим елементом ерадикаційної терапії є ефективна кислотосупресія – використання засобів, які пригнічують кислототвірну функцію шлунка.
У прогнозуванні ефективності антихелікобактерної терапії у конкретного пацієнта потрібно враховувати, з одного боку, ситуацію з резистентністю до антибіотиків (кларитроміцину та метронідазолу) в даному географічному регіоні, з іншого – анамнез використання раніше антибіотиків.
Оскільки терапія, що містить 2 або 3 антибіотики, залежно від клінічного випадку триває 10 або 14 днів, у хворого може розвинутись дисбіоз порожнинного вмісту товстої кишки. Дана терапія повинна проводитись лише під ретельним наглядом лікаря. Наслідком, який найчастіше виникає внаслідок безконтрольного вживання антибіотиків, є антибіотикасоційована діарея та інші прояви дисбіозу, які потребують додаткового, досить тривалого лікування. Для профілактики дисбіозу товстої кишки при ерадикації H. pylori та інших випадках застосування антибіотиків рекомендують вживання пробіотиків – препаратів, що містять лакто- та біфідобактерії або сахароміцети Буларді з першого дня антибіотикотерапії упродовж усього курсу.
Нехай весна принесе лише радість, надії на краще і забезпечить міцне здоров’я.
Матеріал підготували: завідувач кафедри внутрішньої медицини, клінічної фармакології та професійних хвороб, д.м.н., професор Хухліна О.С., асистент кафедри, к.м.н. Дудка Т.В.