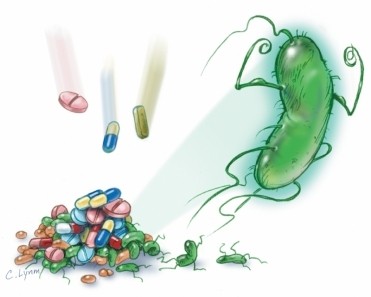
Проблема антибіотикорезистентності в останні роки набуває особливої актуальності у практичній медицині, тому це питання активно вивчається у світовій науці. Що вже відомо?
В еволюції антибіотикорезистентності плазміди та кон’югативні транспозони виконують функцію генетичних платформ, на яких за допомогою рекомбінаційних систем бактерій відбувається збір і сортування генів антибіотикорезистентності, включених у транспозони, інтегрони, генні касети та інсерційні криптичні послідовності.
До теперішнього часу відомо не менше чотирьох біохімічних механізмів, що відповідають за розвиток у бактерій антибіотикорезистентності: детоксикація антибіотика; зменшення проникності стінки мікроорганізму для антибіотиків і / або викачування його з клітини; структурні зміни в молекулах, які є мішенями для антибіотиків; продукція альтернативних мішеней для антибіотиків. Високі рівні антибіотикорезистентності у грамнегативних бактерій обумовлені їх здатністю детоксикувати антибіотики в периплазматичному просторі.
У клітинній стінці грампозитивних бактерій периплазма відсутня, тому механізми їх детоксикаційної резистентності до антибіотиків менш ефективні, ніж у грамнегативних бактерій.
Окремі механізми придбаної стійкості мікробів до лікарняного середовища добре вивчені. Так, японськими вченими Ochiai і Aciba в 1959-1960 рр.. були відкриті гени стійкості до антибіотиків плазміди. Плазміди резистентності до антибіотиків являють собою молекулу ДНК, розташовану в цитоплазмі або ядрі мікробної клітини. Частина плазми (R-фактор) містить гени стійкості до антибіотиків, здатні передавати її не тільки в межах одного виду, а й різних родів і сімейств бактерій. Наприклад, стійкість до антибіотиків може поширюватися від ешерихій до клебсіелли, синьогнійної палички і навпаки. Під дією антибіотика R-плазміди можуть утворюватися і в нормальній природній мікрофлорі кишечника, яка, як встановлено, може служити сховищем стійкості і передавати ці фактори патогенним мікроорганізмам. Виявлення в стаціонарі штаму-носія R-плазмід із багатьма маркерами стійкості, здатними до міжродового переносу, слід вважати несприятливим для стаціонару.
Нещодавно механізм стійкості бактерій до хіміопрепаратів був доповнений відкриттям мобільних генів – транспозони, окремих фрагментів ДНК, здатних до переміщення від однієї молекули до іншої.
Для формування госпітальних штамів збудників має значення здатність транспозонів одночасно зі стійкістю передавати гени, що визначають ряд факторів патогенності і деякі нові біохімічні властивості бактерій, що дозволяють їм довго зберігатися в навколишньому середовищі. Стійкість до антибіотиків ентеробактерій пов’язана в основному присутністю ферменту β-лактамази, ферменту, що розщеплює β-лактамне кільце пеніцилінів та цефалоспоринів. Збудником госпітальної інфекції може бути умовно-патогенний збудник як ендогенного, так і екзогенного походження. При тривалій циркуляції в стаціонарі риси госпітального штаму набувають і безумовно патогенні збудники.
Зважаючи на проблему антибіотикорезистентності, вчені закликають ввести жорсткі обмеження на викиди антибіотиків в рідких відходах фармацевтичного виробництва, сільського господарства і лікарень. Інакше антибіотики продовжать у масовому порядку потрапляти у воду і грунт, що стимулює розвиток генів резистентності (опірності). Також дослідники закликають різко скоротити використання антибактеріальних препаратів у сільському господарстві. Зараз тваринам вводять невеликі дози антибіотиків для стимуляції їхнього росту, що майже не вбиває бактерії, але дозволяє їм посилити опірність. Згідно останніх даних, ген стійкості до антибіотиків, який був виявлений у свиней, м’ясі бройлерів, а також у людей в Китаї, віднедавна виявлений і в Данії. Новий ген стійкості, так званий mcr-1, набуває резистентності до колістину, роду протимікробних поліміксинів, які в останній час використовуються для лікування інфекцій викликаних Г (-) бактеріями, такими як E.Coli і Klebsiella. Приблизно3000 Г(-) бактерії (раніше були відображені в базі даних за допомогою секвенування геному) були переглянуті, щоб побачити, чи присутній в них ген mcr-1. Результати показують, що ген mcr-1 був знайдений у одного пацієнта, який страждав від зараження крові в 2015 році, в п’яти зразках харчових продуктів, які були імпортовані у 2012-2014. Всі ці бактерії були полірезистентні та містили ген mcr-1, який може ще більше ускладнити лікування. Звичайно, це лише поодинокі випадки з тисяч, які однак потребують ретельного вивчення з урахуванням новітніх даних щодо генів резистентності.
Матеріал підготувала: Гулей Лілія – асистент кафедри дерматовенерології, к.мед.н.